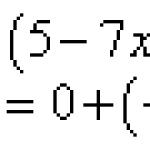Полная характеристика хлора. Хлор очень сильный окислитель. Физические и физико-химические свойства
В природе хлор встречается в газообразном состоянии и только в виде соединений с другими газами. В условиях, приближенных к нормальным, это ядовитый едкий газ зеленоватого цвета. Имеет больший вес, чем воздух. Обладает сладким запахом. Молекула хлора содержит два атома. В спокойном состоянии не горит, но при высоких температурах входит во взаимодействие с водородом, после чего возможен взрыв. В результате выделяется газ фосген. Очень ядовит. Так, даже при малой концентрации в воздухе (0,001 мг на 1 дм 3) может вызвать летальный исход. хлора гласит, что он тяжелее воздуха, следовательно, всегда будет находиться у самого пола в виде желтовато-зеленой дымки.
Исторические факты
Впервые на практике это вещество было получено К. Шелее в 1774 г. путем соединения соляной кислоты и пиролюзита. Однако лишь в 1810 г. П. Дэви смог дать характеристику хлору и установить, что это отдельный химический элемент.
Стоит отметить, что в 1772 г. смог получить хлороводород - соединение хлора с водородом, однако разделить эти два элемента химик не смог.
Химическая характеристика хлора
Хлор - химический элемент основной подгруппы VII группы таблицы Менделеева. Находится в третьем периоде и имеет атомный номер 17 (17 протонов в атомном ядре). Химически активный неметалл. Обозначается буквами Cl.
Является типичным представителем газы, не имеющие цвета, но обладающие резким едким запахом. Как правило, токсичны. Все галогены хорошо разбавляются в воде. При контакте с влажным воздухом начинают дымиться.
Внешняя электронная конфигурация атома Cl 3s2Зр5. Следовательно, в соединениях химический элемент проявляет уровни окисления -1,+1, +3, +4, +5, +6 и +7. Ковалентный радиус атома 0,96Å, ионный радиус Cl- 1.83 Å, сродство атома к электрону 3,65 эв, уровень ионизации 12,87 эв.
Как указано выше, хлор представляет собой довольно активный неметалл, что позволяет создавать соединения практически с любыми металлами (в отдельных случаях при помощи нагревания или с помощью влаги, вытесняя при этом бром) и неметаллами. В порошкообразной форме реагирует с металлами только под действием высоких температур.
Максимальная температура горения - 2250 °С. С кислородом способен образовывать оксиды, гипохлориты, хлориты и хлораты. Все соединения, содержащие кислород, становятся взрывоопасными в условиях взаимодействия с окисляющимися веществами. Стоит отметить, что могут произвольно взрываться, в то время как хлораты взрываются лишь при воздействии на них какими-либо инициаторами.
Характеристика хлора по положению в периодической системе:
Простое вещество;
. элемент семнадцатой группы периодической таблицы;
. третий период третьего ряда;
. седьмая группа главной подгруппы;
. атомный номер 17;
. обозначается символом Cl;
. химически активный неметалл;
. находится в группе галогенов;
. в условиях, приближенных к нормальным, это ядовитый газ желтовато-зелёного цвета с едким запахом;
. молекула хлора имеет 2 атома (формула Cl 2).

Физические свойства хлора:
Температура кипения: -34,04 °С;
. температура плавления: -101,5 °С;
. плотность в газообразном состоянии - 3 ,214 г/л;
. плотность жидкого хлора (в период кипения) - 1,537 г/см 3 ;
. плотность твердого хлора - 1,9 г/см 3 ;
. удельный объем - 1,745 х 10 -3 л/г.
Хлор: характеристика температурных изменений
В газообразном состоянии имеет свойство легко сжижаться. При давлении в 8 атмосфер и температуре 20 °С выглядит как зеленовато-желтая жидкость. Обладает очень высокими коррозионными свойствами. Как показывает практика, этот химический элемент может сохранять жидкое состояние вплоть до критической температуры (143 °С), при условии увеличения давления.
Если его охладить до температуры -32 °С, он изменит свое на жидкое вне зависимости от атмосферного давления. При дальнейшем понижении температуры происходит кристаллизация (при показателе -101 °С).

Хлор в природе
В земной коре хлора содержится всего 0,017 %. Основная масса находится в вулканических газах. Как указано выше, вещество имеет большую химическую активность, вследствие чего в природе встречается в соединениях с другими элементами. При этом множество минералов содержат хлор. Характеристика элемента позволяет образовывать порядка ста различных минералов. Как правило, это хлориды металлов.
Также большое его количество находится в Мировом океане - почти 2 %. Это обусловлено тем, что хлориды очень активно растворяются и разносятся с помощью рек и морей. Возможен и обратный процесс. Хлор вымывается обратно на берег, а далее ветер разносит его по окрестностям. Именно поэтому наибольшая его концентрация наблюдается в прибрежных зонах. В засушливых районах планеты рассматриваемый нами газ образуется при помощи испарения воды, вследствие чего появляются солончаки. Ежегодно в мире добывают порядка 100 млн тонн данного вещества. Что, впрочем, неудивительно, ведь существует много месторождений, содержащих хлор. Характеристика его, однако, во многом зависит именно от его географического положения.
Методы получения хлора
Сегодня существует ряд методов получения хлора, из которых наиболее распространены следующие:
1. Диафрагменный. Является самым простым и менее затратным. Соляной раствор в диафрагменном электролизе поступает в пространство анода. Далее по стальной катодной сетке перетекает в диафрагму. В ней находится небольшое количество полимерных волокон. Важной особенностью этого устройства является противоток. Он направлен из анодного пространства в катодное, что позволяет отдельно получить хлор и щелоки.
2. Мембранный. Наиболее энергоэффективен, но сложноосуществим в организации. Схож с диафрагменным. Различие состоит в том, что анодное и катодное пространства полностью разделены мембраной. Следовательно, на выходе получаются два отдельных потока.
Стоит отметить, что характеристика хим. элемента (хлора), полученного данными методами, будет иной. Более "чистым" принято считать мембранный метод.
3. Ртутный метод с жидким катодом. По сравнению с остальными технологиями, этот вариант позволяет получать наиболее чистый хлор.
Принципиальная схема установки состоит из электролизера и соединенных между собой насоса и разлагателя амальгамы. В качестве катода служит перекачиваемая насосом ртуть вместе с раствором поваренной соли, а в качестве анода - угольные или графитовые электроды. Принцип действия установки следующий: из электролита выделяется хлор, который отводится из электролизера вместе с анолитом. Из последнего удаляют примеси и остатки хлора, донасыщают галитом и снова возвращают на электролиз.
Требования промышленной безопасности и нерентабельность производства привели к замене жидкого катода твердым.

Применение хлора в промышленных целях
Свойства хлора позволяют активно применять его в промышленности. С помощью этого химического элемента получают различные (винилхлорид, хлоро-каучук и др.), лекарственные препараты, дезинфицирующие средства. Но самая большая ниша, занятая в промышленности, это производство соляной кислоты и извести.
Широко применяются методы очищения питьевой воды. На сегодняшний день пытаются отойти от этого метода, заменив его озонированием, поскольку рассматриваемое нами вещество негативно влияет на организм человека, к тому же хлорированная вода разрушает трубопроводы. Вызвано это тем, что в свободном состоянии Cl пагубно влияет на трубы, изготовленные из полиолефинов. Тем не менее большинство стран отдает предпочтение именно методу хлорирования.

Также хлор применяется в металлургии. С его помощью получают ряд редких металлов (ниобий, тантал, титан). В химической промышленности активно используют различные хлорорганические соединения для борьбы против сорняков и для других сельскохозяйственных целей, используется элемент и в качестве отбеливателя.
Благодаря своей химической структуре хлор разрушает большинство органических и неорганических красителей. Достигается это путем полного их обесцвечивания. Такой результат возможен лишь при условии присутствия воды, ведь процесс обесцвечивания происходит благодаря который образуется после распада хлора: Cl 2 + H 2 O → HCl + HClO → 2HCl + O. Данный способ нашел применение пару веков назад и пользуется популярностью и по сей день.
Очень популярно применение этого вещества для получения хлорорганических инсектицидов. Эти сельскохозяйственные препараты убивают вредоносные организмы, оставляя нетронутыми растения. Значительная часть всего добываемого на планете хлора уходит на сельскохозяйственные нужды.

Также используется он при производстве пластикатов и каучука. С их помощью изготавливают изоляцию проводов, канцелярские товары, аппаратуру, оболочки бытовой техники и т. д. Бытует мнение, что каучуки, полученные таким образом, вредят человеку, но это не подтверждено наукой.
Стоит отметить, что хлор (характеристика вещества была подробно раскрыта нами ранее) и его производные, такие как иприт и фосген, применяются и в военных целях для получения боевых отравляющих средств.
Хлор как яркий представитель неметаллов
Неметаллы - простые вещества, которые включают в себя газы и жидкости. В большинстве случаев они хуже проводят электрический ток, чем металлы, и имеют существенные различия в физико-механических характеристиках. При помощи высокого уровня ионизации способны образовывать ковалентные химические соединения. Ниже будет дана характеристика неметалла на примере хлора.
Как уже было сказано выше, этот химический элемент представляет собой газ. В нормальных условиях у него полностью отсутствуют свойства, сходные с таковыми у металлов. Без сторонней помощи не может взаимодействовать с кислородом, азотом, углеродом и др. Свои окислительные свойства проявляет в связях с простыми веществами и некоторыми сложными. Относится к галогенам, что ярко отражается на его химических особенностях. В соединениях с остальными представителями галогенов (бром, астат, йод), вытесняет их. В газообразном состоянии хлор (характеристика его - прямое тому подтверждение) хорошо растворяется. Является отличным дезинфектором. Убивает только живые организмы, что делает его незаменимым в сельском хозяйстве и медицине.
Применение в качестве отравляющего вещества
Характеристика атома хлора позволяет применять его как отравляющее средство. Впервые газ был применен Германией 22.04.1915 г., в ходе Первой мировой войны, вследствие чего погибло порядка 15 тыс. человек. На данный момент как не применяется.
Дадим краткую характеристику химического элемента как удушающего средства. Влияет на организм человека посредством удушения. Сначала оказывает раздражение верхних дыхательных путей и слизистой оболочки глаз. Начинается сильный кашель с приступами удушья. Далее, проникая в легкие, газ разъедает легочную ткань, что приводит к отеку. Важно! Хлор является быстродействующим веществом.
В зависимости от концентрации в воздухе, симптоматика бывает разной. При малом содержании у человека наблюдается покраснение слизистой оболочки глаз, легкая одышка. Содержание в атмосфере 1,5-2 г/м 3 вызывает тяжесть и острые ощущения в груди, резкую боль в верхних дыхательных путях. Также состояние может сопровождаться сильным слезотечением. После 10-15 минут нахождения в помещении с такой концентрацией хлора наступает сильный ожог легких и смерть. При более плотных концентрациях смерть возможна в течение минуты от паралича верхних дыхательных путей.

Хлор в жизни организмов и растений
Хлор входит в состав практически всех живых организмов. Особенность состоит в том, что присутствует он не в чистом виде, а в виде соединений.
В организмах животных и человека ионы хлора поддерживают осмотическое равенство. Вызвано это тем, что они имеют наиболее подходящий радиус для проникновения в мембранные клетки. Наряду с ионами калия Cl регулирует водно-солевой баланс. В кишечнике ионы хлора создают благоприятную среду для действия протеолитических ферментов желудочного сока. Хлорные каналы предусмотрены во многих клетках нашего организма. Посредством их происходит межклеточный обмен жидкостями и поддерживается pH клетки. Порядка 85 % от общего объема этого элемента в организме пребывает в межклеточном пространстве. Выводится из организма по мочеиспускательным каналам. Вырабатывается женским организмом в процессе кормления грудью.
На данном этапе развития тяжело однозначно сказать, какие именно заболевания провоцирует хлор и его соединения. Связано это с недостатком исследований в этой области.
Также ионы хлора присутствуют в клетках растений. Он активно принимает участие в энергетическом обмене. Без этого элемента невозможен процесс фотосинтеза. С его помощью корни активно впитывают необходимые вещества. Но большая концентрация хлора в растениях способна оказывать пагубное влияние (замедление процесса фотосинтеза, остановка развития и роста).

Однако существуют такие представители флоры, которые смогли "подружиться" или хотя бы ужиться с данным элементом. Характеристика неметалла (хлора) содержит такой пункт, как способность вещества окислять почвы. В процессе эволюции упомянутые выше растения, называемые галофитами, заняли пустые солончаки, которые пустовали из-за переизбытка этого элемента. Они впитывают ионы хлора, а после избавляются от них при помощи листопада.
Транспортировка и хранение хлора
Существует несколько способов перемещать и хранить хлор. Характеристика элемента предполагает необходимость специальных баллонов с высоким давлением. Такие емкости имеют опознавательную маркировку - вертикальную зеленую линию. Ежемесячно баллоны необходимо тщательно промывать. При длительном хранении хлора в них образуется очень взрывоопасный осадок - трихлорид азота. При несоблюдении всех правил безопасности возможно самопроизвольное воспламенение и взрыв.

Изучение хлора
Будущим химикам должна быть известна характеристика хлора. По плану 9-классники могут даже ставить лабораторные опыты с этим веществом на основе базовых знаний по дисциплине. Естественно, преподаватель обязан провести инструктаж по технике безопасности.
Порядок работ следующий: необходимо взять колбу с хлором и насыпать в неё мелкую металлическую стружку. В полете стружка вспыхнет яркими светлыми искрами и одновременно образуется легкий белый дым SbCl 3 . При погружении в сосуд с хлором оловянной фольги она также самовоспламенится, а на дно колбы медленно опустятся огненные снежинки. Во время этой реакции образуется дымная жидкость - SnCl 4 . При помещении железной стружки в сосуде образуются красные «капли» и появится рыжий дым FeCl 3 .
Наряду с практическими работами повторяется теория. В частности, такой вопрос, как характеристика хлора по положению в периодической системе (описана в начале статьи).

В результате опытов выясняется, что элемент активно реагирует на органические соединения. Если поместить в банку с хлором вату, смоченную предварительно в скипидаре, то она мгновенно воспламенится, и из колбы резко повалит сажа. Эффектно тлеет желтоватым пламенем натрий, а на стенках химпосуды появляются кристаллы соли. Ученикам будет небезынтересно узнать, что, будучи ещё молодым химиком, Н. Н. Семенов (впоследствии лауреат Нобелевской премии), проведя такой опыт, собрал со стенок колбы соль и, посыпав ею хлеб, съел его. Химия оказалась права и не подвела ученого. В результате проведенного химиком опыта действительно получилась обычная поваренная соль!
На западе Фландрии лежит крошечный городок. Тем не менее его название известно всему миру и долго еще будет сохраняться в памяти человечества как символ одного из величайших преступлений против человечества. Этот городок – Ипр. Креси (в битве при Креси в 1346 г. английскими войсками впервые в Европе применено огнестрельное оружие.) – Ипр – Хиросима – вехи на пути превращения войны в гигантскую машину уничтожения.
В начале 1915 г. на линии западного фронта образовался так называемый Ипрский выступ. Союзные англо-французские войска к северо-востоку от Ипра вклинились на территорию, запятую германской армией. Германское командование решило нанести контрудар и выровнять линию фронта. Утром 22 апреля, когда дул ровный норд-ост, немцы начали необычную подготовку к наступлению – они провели первую в истории войн газовую атаку. На ипрском участке фронта были одновременно открыты 6000 баллонов хлора. В течение пяти минут образовалось огромное, весом в 180 т, ядовитое желто-зеленое облако, которое медленно двигалось по направлению к окопам противника.
Этого никто не ожидал. Войска французов и англичан готовились к атаке, к артиллерийскому обстрелу, солдаты надежно окопались, но перед губительным хлорным облаком они были абсолютно безоружными. Смертоносный газ проникал во все щели, во все укрытия. Результаты первой химической атаки (и первого нарушения Гаагской конвенции 1907 г. о неприменении отравляющих веществ!) были ошеломляющими – хлор поразил около 15 тысяч человек, причем примерно 5 тысяч – на смерть. И все это – ради того, чтобы выровнять линию фронта длиной в 6 км! Спустя два месяца немцы предприняли хлорную атаку и на восточном фронте. А через два года Ипр приумножил свою печальную известность. Во время тяжелого сражения 12 июля 1917 г. в районе этого города было впервые применено отравляющее вещество, названное впоследствии ипритом. Иприт – это производное хлора, дихлордиэтилсульфид.
Об этих эпизодах истории, связанных с одним маленьким городком и одним химическим элементом, мы напомнили для того, чтобы показать, как опасен может быть элемент №17 в руках воинствующих безумцев. Это – самая мрачная страница истории хлора.
Но было бы совершенно неверно видеть в хлоре только отравляющее вещество и сырье для производства других отравляющих веществ...
История хлора
История элементарного хлора сравнительно коротка, она ведет начало с 1774 г. История соединений хлора стара, как мир. Достаточно вспомнить, что хлористый натрий – это поваренная соль. И, видимо, еще в доисторические времена была подмечена способность соли консервировать мясо и рыбу.
Самые древние археологические находки – свидетельства использования соли человеком относятся примерно к 3...4 тысячелетию до н.э. А самое древнее описание добычи каменной соли встречается в сочинениях греческого историка Геродота (V в. до н.э.). Геродот описывает добычу каменной соли в Ливии. В оазисе Синах в центре Ливийской пустыни находился знаменитый храм бога Аммона-Ра. Поэтому-то Ливия и именовалась «Ammonia», и первое название каменной соли было «sal ammoniacum». Позднее, начиная примерно с XIII в. н.э., это название закрепилось за хлористым аммонием.
В «Естественной истории» Плиния Старшего описан метод отделения золота от неблагородных металлов при прокаливании с солью и глиной. А одно из первых описаний очистки хлористого натрия находим в трудах великого арабского врача и алхимика Джабир ибн-Хайяна (в европейском написании – Гебер).
Весьма вероятно, что алхимики сталкивались и с элементарным хлором, так как в странах Востока уже в IX, а в Европе в XIII в. была известна «царская водка» – смесь соляной и азотной кислот. В выпущенной в 1668 г. книге голландца Ван-Гельмонта «Hortus Medicinae» говорится, что при совместном нагревании хлористого аммония и азотной кислоты получается некий газ. Судя по описанию, этот газ очень похож на хлор.
Подробно хлор впервые описан шведским химиком Шееле в его трактате о пиролюзите. Нагревая минерал пиролюзит с соляной кислотой, Шееле заметил запах, характерный для царской водки, собрал и исследовал желто-зеленый газ, порождавший этот запах, и изучил его взаимодействие с некоторыми веществами. Шееле первым обнаружил действие хлора на золото и киноварь (в последнем случае образуется сулема) и отбеливающие свойства хлора.
Шееле не считал вновь открытый газ простым веществом и назвал его «дефлогистонированной соляной кислотой». Говоря современным языком, Шееле, а вслед за ним и другие ученые того времени полагали, что новый газ – это окисел соляной кислоты.
Несколько позже Бертоле и Лавуазье предложили считать этот газ окислом некоего нового элемента «мурия». В течение трех с половиной десятилетий химики безуспешно пытались выделить неведомый мурий.
Сторонником «окиси мурия» был поначалу и Дэви, который в 1807 г. разложил электрическим током поваренную соль на щелочной металл натрий и желто-зеленый газ. Однако, спустя три года, после многих бесплодных попыток получить мурий Дэви пришел к выводу, что газ, открытый Шееле, – простое вещество, элемент, и назвал его chloric gas или chlorine (от греческого χλωροζ – желто-зеленый). А еще через три года Гей-Люссак дал новому элементу более короткое имя – хлор. Правда, еще в 1811 г. немецкий химик Швейгер предложил для хлора другое название – «галоген» (дословно оно переводится как солерод), но это название поначалу не привилось, а впоследствии стало общим для целой группы элементов, в которую входит и хлор.
«Личная карточка» хлора
На вопрос, что же такое хлор, можно дать минимум десяток ответов. Во-первых, это галоген; во-вторых, один из самых сильных окислителей; в-третьих, чрезвычайно ядовитый газ; в-четвертых, важнейший продукт основной химической промышленности; в-пятых, сырье для производства пластмасс и ядохимикатов, каучука и искусственного волокна, красителей и медикаментов; в-шестых, вещество, с помощью которого получают титан и кремний, глицерин и фторопласт; в-седьмых, средство для очистки питьевой воды и отбеливания тканей...
Это перечисление можно было бы продолжить.
При обычных условиях элементарный хлор – довольно тяжелый желто-зеленый газ с резким характерным запахом. Атомный вес хлора 35,453, а молекулярный – 70,906, потому что молекула хлора двухатомна. Один литр газообразного хлора при нормальных условиях (температура 0°C и давление 760 мм ртутного столба) весит 3,214 г. При охлаждении до температуры –34,05°C хлор конденсируется в желтую жидкость (плотностью 1,56 г/см 3), а при температуре – 101,6°C затвердевает. При повышенном давлении хлор можно превратить в жидкость и при более высоких температурах вплоть до +144°C. Хлор хорошо растворяется в дихлорэтане и некоторых других хлорсодержащих органических растворителях.
Элемент №17 очень активен – он непосредственно соединяется почти со всеми элементами периодической системы. Поэтому в природе он встречается только в виде соединений. Самые распространенные минералы, содержащие хлор, галит NaCI, сильвинит KCl · NaCl, бишофит MgCl 2 · 6H 2 O, карналлит KCl · MgCl 2 · 6Н 2 O, каинит KCl · МgSO 4 · 3Н 2 О. Это их в первую очередь «вина» (или «заслуга»), что содержание хлора в земной коре составляет 0,20% по весу. Для цветной металлургии очень важны некоторые относительно редкие хлорсодержащие минералы, например роговое серебро AgСl.
По электропроводности жидкий хлор занимает место среди самых сильных изоляторов: он проводит ток почти в миллиард раз хуже, чем дистиллированная вода, и в 10 22 раз хуже серебра.
Скорость звука в хлоре примерно в полтора раза меньше, чем в воздухе.
И напоследок – об изотопах хлора.
Сейчас известны девять изотопов этого элемента, но в природе встречаются только два – хлор-35 и хлор-37. Первого примерно в три раза больше, чем второго.
Остальные семь изотопов получены искусственно. Самый короткоживущий из них – 32 Cl имеет период полураспада 0,306 секунды, а самый долгоживущий – 36 Cl – 310 тыс. лет.
Как получают хлор
Первое, на что обращаешь внимание, попав на хлорный завод, это многочисленные линии электропередачи. Хлорное производство потребляет много электроэнергии – она нужна для того, чтобы разложить природные соединения хлора.
Естественно, что основное хлорное сырье – это каменная соль. Если хлорный завод расположен вблизи реки, то соль завозят не по железной дороге, а на баржах – так экономичнее. Соль – продукт недорогой, а расходуется ее много: чтобы получить тонну хлора, нужно примерно 1,7...1,8 т соли.
Соль поступает на склады. Здесь хранятся трех – шестимесячные запасы сырья – хлорное производство, как правило, многотоннажное.
Соль измельчают и растворяют в теплой воде. Этот рассол по трубопроводу перекачивается в цех очистки, где в огромных, высотой с трехэтажный дом баках рассол очищают от примесей солей кальция и магния и осветляют (дают ему отстояться). Чистый концентрированный раствор хлористого натрия перекачивается в основной цех хлорного производства – в цех электролиза.
В водном растворе молекулы поваренной соли превращаются в ионы Na + и Сl – . Ион Сl – отличается от атома хлора только тем, что имеет один лишний электрон. Значит, для того чтобы получить элементарный хлор, необходимо оторвать этот лишний электрон. Происходит это в электролизере на положительно заряженном электроде (аноде). С него как бы «отсасываются» электроны: 2Cl – → Cl 2 + 2ē . Аноды сделаны из графита, потому что любой металл (кроме платины и ее аналогов), отбирая у ионов хлора лишние электроны, быстро корродирует и разрушается.
Существуют два типа технологического оформления производства хлора: диафрагменный и ртутный. В первом случае катодом служит перфорированный железный лист, а катодное и анодное пространства электролизера разделены асбестовой диафрагмой. На железном катоде происходит разряд ионов водорода и образуется водный раствор едкого натра. Если в качестве катода применяют ртуть, то на нем разряжаются ионы натрия и образуется амальгама натрия, которая потом разлагается водой. Получаются водород и едкий натр. В этом случае разделительная диафрагма не нужна, а щелочь получается более концентрированной, чем в диафрагменных электролизерах.
Итак, производство хлора – это одновременно производство едкого натра и водорода.
Водород отводят по металлическим, а хлор по стеклянным или керамическим трубам. Свежеприготовленный хлор насыщен парами воды и потому особенно агрессивен. В дальнейшем его сначала охлаждают холодной водой в высоких башнях, выложенных изнутри керамическими плитками и наполненных керамической насадкой (так называемыми кольцами Рашига), а затем сушат концентрированной серной кислотой. Это единственный осушитель хлора и одна из немногих жидкостей, с которыми хлор но взаимодействует.
Сухой хлор уже не так агрессивен, он не разрушает, например, стальную аппаратуру.
Транспортируют хлор обычно в жидком состоянии в железнодорожных цистернах или баллонах под давлением до 10 атм.
В России производство хлора было впервые организовано еще в 1880 г. на Бондюжском заводе. Хлор получали тогда в принципе тем же способом, каким в свое время получил его Шееле – при взаимодействии соляной кислоты с пиролюзитом. Весь производимый хлор расходовался на получение хлорной извести. В 1900 г. на заводе «Донсода» впервые в России был введен в эксплуатацию цех электролитического производства хлора. Мощность этого цеха была всего 6 тыс. т в год. В 1917 г. все хлорные заводы России выпускали 12 тыс. т хлора. А в 1965 г. в СССР было произведено около 1 млн т хлора...
Один из многих
Все многообразие практического применения хлора можно без особой натяжки выразить одной фразой: хлор необходим для производства хлорпродуктов, т.е. веществ, содержащих «связанный» хлор. А вот говоря об этих самых хлорпродуктах, одной фразой не отделаешься. Они очень разные – и по свойствам, и по назначению.
Рассказать обо всех соединениях хлора не позволяет ограниченный объем нашей статьи, но без рассказа хотя бы о некоторых веществах, для получения которых нужен хлор, наш «портрет» элемента №17 был бы неполным и неубедительным.
Взять, к примеру, хлорорганические инсектициды – вещества, убивающие вредных насекомых, но безопасные для растений. На получение средств защиты растений расходуется значительная часть производимого хлора.
Один из самых важных инсектицидов – гексахлорциклогексан (часто называемый гексахлораном). Это вещество впервые синтезировано еще в 1825 г. Фарадеем, но практическое применение нашло только через 100 с лишним лет – в 30-х годах нашего столетия.
Сейчас гексахлоран получают, хлорируя бензол. Подобно водороду, бензол очень медленно реагирует с хлором в темноте (и в отсутствие катализаторов), но при ярком освещении реакция хлорирования бензола (С 6 Н 6 + 3Сl 2 → С 6 Н 6 Сl 6) идет достаточно быстро.
Гексахлоран, так же как и многие другие инсектициды, применяется в виде дустов с наполнителями (тальком, каолином), или в виде суспензий и эмульсий, или, наконец, в виде аэрозолей. Гексахлоран особенно эффективен при протравливании семян и при борьбе с вредителями овощных и плодовых культур. Расход гексахлорана составляет всего 1...3 кг на гектар, экономический эффект от его применения в 10...15 раз превосходит затраты. К сожалению, гексахлоран не безвреден для человека...
Поливинилхлорид
Если попросить любого школьника перечислить известные ему пластики, он одним из первых назовет поливинилхлорид (иначе, винипласт). С точки зрения химика, ПВХ (так часто поливинилхлорид обозначают в литературе) – это полимер, в молекуле которого на цепочку углеродных атомов «нанизаны» атомы водорода и хлора:
В этой цепочке может быть несколько тысяч звеньев.
А с потребительской точки зрения ПВХ – это изоляция для проводов и плащи-дождевики, линолеум и граммпластинки, защитные лаки и упаковочные материалы, химическая аппаратура и пенопласты, игрушки и детали приборов.
Поливинилхлорид образуется при полимеризации винилхлорида, который чаще всего получают, обрабатывая ацетилен хлористым водородом: HC ≡ CH + HCl → CH 2 = CHCl. Существует и другой способ получения винилхлорида – термический крекинг дихлорэтана.
CH 2 Cl – CH 2 Сl → CH 2 = CHCl + HCl. Представляет интерес сочетание двух этих методов, когда в производстве винилхлорида по ацетиленовому способу используют HCl, выделяющийся при крекинге дихлорэтана.
Хлористый винил – бесцветный газ с приятным, несколько пьянящим эфирным запахом, легко полимеризуется. Для получения полимера жидкий винилхлорид под давлением нагнетают в теплую воду, где он дробится на мельчайшие капельки. Чтобы они не сливались, в воду добавляют немного желатины или поливинилового спирта, а чтобы начала развиваться реакция полимеризации, туда же вводят инициатор полимеризации – перекись бензоила. Через несколько часов капельки затвердевают, и образуется суспензия полимера в воде. Порошок полимера отделяют на фильтре или на центрифуге.
Полимеризация обычно происходит при температуре от 40 до 60°C, причем, чем ниже температура полимеризации, тем длиннее образующиеся полимерные молекулы...
Мы рассказали только о двух веществах, для получения которых необходим элемент №17. Только о двух из многих сотен. Подобных примеров можно привести очень много. И все они говорят о том, что хлор – это не только ядовитый и опасный газ, но очень важный, очень полезный элемент.
Элементарный расчет
При получении хлора электролизом раствора поваренной соли одновременно получаются водород и едкий натр: 2NACl + 2H 2 О = H 2 + Cl 2 + 2NaOH. Конечно, водород – очень важный химический продукт, но есть более дешевые и удобные способы производства этого вещества, например конверсия природного газа... А вот едкий натр получают почти исключительно электролизом растворов поваренной соли – на долю других методов приходится меньше 10%. Поскольку производства хлора и NaOH полностью взаимосвязаны (как следует из уравнения реакции, получение одной грамм-молекулы – 71 г хлора – неизменно сопровождается получением двух грамм-молекул – 80 г электролитической щелочи), зная производительность цеха (или завода, или государства) по щелочи, можно легко рассчитать, сколько хлора он производит. Каждой тонне NaOH «сопутствуют» 890 кг хлора.
Ну и смазка!
Концентрированная серная кислота – практически единственная жидкость, не взаимодействующая с хлором. Поэтому для сжатия и перекачивания хлора на заводах используют насосы, в которых роль рабочего тела и одновременно смазки выполняет серная кислота.
Псевдоним Фридриха Вёлера
Исследуя взаимодействие органических веществ с хлором, французский химик XIX в. Жан Дюма сделал поразительное открытие: хлор способен замещать водород в молекулах органических соединений. Например, при хлорировании уксусной кислоты сначала один водород метильной группы замещается на хлор, затем другой, третий... Но самым поразительным было то, что по химическим свойствам хлоруксусные кислоты мало чем отличались от самой уксусной кислоты. Обнаруженный Дюма класс реакций был совершенно необъясним господствовавшими в то время электрохимической гипотезой и теорией радикалов Берцелиуса (по выражению французского химика Лорана, открытие хлоруксусной кислоты было подобно метеору, который разрушил всю старую школу). Берцелиус, его ученики и последователи бурно оспаривали правильность работ Дюма. В немецком журнале «Annalen der Chemie und Pharmacie» появилось издевательское письмо знаменитого немецкого химика Фридриха Вёлера под псевдонимом S.С.Н. Windier (по немецки «Schwindler» значит «лжец», «обманщик»). В нем сообщалось, что автору удалось заместить в клетчатке (С 6 Н 10 O 5) и все атомы углерода. водорода и кислорода на хлор, причем свойства клетчатки при этом не изменились. И что теперь в Лондоне делают теплые набрюшники из ваты, состоящей... из чистого хлора.
Хлор и вода
Хлор заметно растворяется в воде. При 20°C в одном объеме воды растворяется 2,3 объема хлора. Водные растворы хлора (хлорная вода) – желтого цвета. Но со временем, особенно при хранении на свету, они постепенно обесцвечиваются. Объясняется это тем, что растворенный хлор частично взаимодействует с водой, образуются соляная и хлорноватистая кислоты: Cl 2 + H 2 O → HCl + HOCl. Последняя неустойчива и постепенно распадается на HCl и кислород. Поэтому раствор хлора в воде постепенно превращается в раствор соляной кислоты.
Но при низких температурах хлор и вода образуют кристаллогидрат необычного состава – Cl 2 · 5 3 / 4 H 2 O. Эти зеленовато-желтые кристаллы (устойчивые только при температурах ниже 10°C) можно получить, пропуская хлор через воду со льдом. Необычная формула объясняется структурой кристаллогидрата, а она определяется в первую очередь структурой льда. В кристаллической решетке льда молекулы Н 2 О могут располагаться таким образом, что между ними появляются закономерно расположенные пустоты. Элементарная кубическая ячейка содержит 46 молекул воды, между которыми есть восемь микроскопических пустот. В этих пустотах и оседают молекулы хлора. Точная формула кристаллогидрата хлора поэтому должна быть записана так: 8Сl 2 · 46Н 2 О.
Отравление хлором
Присутствие в воздухе уже около 0,0001% хлора раздражающе действует на слизистые оболочки. Постоянное пребывание в такой атмосфере может привести к заболеванию бронхов, резко ухудшает аппетит, придает зеленоватый оттенок коже. Если содержание хлора в воздухе составляет 0,1°/о, то может наступить острое отравление, первый признак которого – приступы сильнейшего кашля. При отравлении хлором необходим абсолютный покой; полезно вдыхать кислород, или аммиак (нюхая нашатырный спирт), или пары спирта с эфиром. По существующим санитарным нормам содержание хлора в воздухе производственных помещений не должно превышать 0,001 мг/л, т.е. 0,00003%.
Не только яд
«Что волки жадны, всякий знает». Что хлор ядовит – тоже. Однако в небольших дозах ядовитый хлор иногда может служить и противоядием. Так, пострадавшим от сероводорода дают нюхать нестойкую хлорную известь. Взаимодействуя, два яда взаимно нейтрализуются.
Анализ на хлор
Для определения содержания хлора пробу воздуха пропускают через поглотители с подкисленным раствором йодистого калия. (Хлор вытесняет йод, количество последнего легко определяется титрованием с помощью раствора Nа 2 S 2 O 3). Для определения микроколичеств хлора в воздухе часто применяется колориметрический метод, основанный на резком изменении окраски некоторых соединений (бензидина, ортотолуидина, метилоранжа) при окислении их хлором. Например, бесцветный подкисленный раствор бензидина приобретает желтый цвет, а нейтральный – синий. Интенсивность окраски пропорциональна количеству хлора.
Кузбасский государственный технический университет
Курсовая работа
Предмет БЖД
Характеристика хлора как аварийно химически опасного вещества
Кемерово-2009
Введение
1. Характеристика АХОВ (по выданному заданию)
2. Способы предотвращения аварии, защита от АХОВ
3. Задание
4. Расчет химической обстановки (по выданному заданию)
Заключение
Литература
Введение
Всего в России функционируют 3300 объектов экономики, располагающих значительными запасами опасных химических веществ. Более 35% из них имеют запасы хора.
Хлор (лат. Chlorum), Cl - химический элемент VII группы периодической системы Менделеева, атомный номер 17, атомная масса 35,453; относится к семейству галогенов.
Xлор применяется также для хлорирования нек оторых руд с целью и влечения титана, ниобия, циркония и других.
Отравления хлором возможны в химической, целлюлозно-бумажной, текстильной, фармацевтичой промышленности. Xлор раздражает слизистые оболочки глаз и дыхательных путей. К первичным воспалительным изменениям обычно присоединяется вторичная инфекция. Острое отравление развивается почти немедленно. При вдыхании средних и низких концентраций хлора отмечаются стеснение и боль в груди, сухой кашель, учащённое дыхание, резь в глазах, слезотечение, повышение содержания лейкоцитов в крови, температуры тела и т. п. Возможны бронхопневмония, токсический отёк лёгких, депрессивные состояния, судороги. В лёгких случаях выздоровление наступает через 3 - 7 суток. Как отдалённые последствия наблюдаются катары верхних дыхательных путей, рецидивирующий бронхит, пневмосклероз; возможна активизация туберкулёза лёгких. При длительном вдыхании небольших концентраций хлора наблюдаются аналогичные, но медленно развивающиеся формы заболевания. Профилактика отравлений, герметизация производств, оборудования, эффективная вентиляция, при необходимости использование противогаза. Предельно допустимая концентрация хлора в воздухе производств, помещений 1 мг/м 3 . Производство хлора, хлорной извести и других хлорсодержащих соединений относится к производствам с вредными условиями труда .
Рассмотрены физические свойства хлора: плотность хлора, его теплопроводность, удельная теплоемкость и динамическая вязкость при различных температурах. Физические свойства Cl 2 представлены в виде таблиц для жидкого, твердого и газообразного состояния этого галогена.
Основные физические свойства хлора
Хлор входит в VII группу третьего периода периодической системы элементов под номером 17. Он относится к подгруппе галогенов, имеет относительные атомную и молекулярные массы 35,453 и 70,906, соответственно. При температурах выше -30°С хлор представляет собой зеленовато-желтый газ с характерным резким раздражающим запахом. Он легко сжижается под обычным давлением (1,013·10 5 Па), будучи охлажден до -34°С, и образует прозрачную жидкость янтарного цвета, затвердевающую при температуре -101°С.
Из-за своей высокой химической активности свободный хлор не встречается в природе, а существует только в форме соединений. Он содержится главным образом в минерале галите (), также входит в состав таких минералов, как: сильвин (KCl), карналлит (KCl·MgCl 2 ·6H 2 O) и сильвинит (KCl·NaCl). Содержание хлора в земной коре приближается к 0,02% от общего числа атомов земной коры, где он находится в виде двух изотопов 35 Cl и 37 Cl в процентном соотношении 75,77% 35 Cl и 24,23% 37 Cl.
| Свойство | Значение |
|---|---|
| Температура плавления, °С | -100,5 |
| Температура кипения, °С | -30,04 |
| Критическая температура, °С | 144 |
| Критическое давление, Па | 77,1·10 5 |
| Критическая плотность, кг/м 3 | 573 |
| Плотность газа (при 0°С и 1,013·10 5 Па), кг/м 3 | 3,214 |
| Плотность насыщенного пара (при 0°С и 3,664·10 5 Па), кг/м 3 | 12,08 |
| Плотность жидкого хлора (при 0°С и 3,664·10 5 Па), кг/м 3 | 1468 |
| Плотность жидкого хлора (при 15,6°С и 6,08·10 5 Па), кг/м 3 | 1422 |
| Плотность твердого хлора (при -102°С), кг/м 3 | 1900 |
| Относительная плотность по воздуху газа (при 0°С и 1,013·10 5 Па) | 2,482 |
| Относительная плотность по воздуху насыщенного пара (при 0°С и 3,664·10 5 Па) | 9,337 |
| Относительная плотность жидкого хлора при 0°С (по воде при 4°С) | 1,468 |
| Удельный объем газа (при 0°С и 1,013·10 5 Па), м 3 /кг | 0,3116 |
| Удельный объем насыщенного пара (при 0°С и 3,664·10 5 Па), м 3 /кг | 0,0828 |
| Удельный объем жидкого хлора (при 0°С и 3,664·10 5 Па), м 3 /кг | 0,00068 |
| Давление паров хлора при 0°С, Па | 3,664·10 5 |
| Динамическая вязкость газа при 20°С, 10 -3 Па·с | 0,013 |
| Динамическая вязкость жидкого хлора при 20°С, 10 -3 Па·с | 0,345 |
| Теплота плавления твердого хлора (при температуре плавления), кДж/кг | 90,3 |
| Теплота парообразования (при температуре кипения), кДж/кг | 288 |
| Теплота сублимации (при температуре плавления), кДж/моль | 29,16 |
| Молярная теплоемкость C p газа (при -73…5727°С), Дж/(моль·К) | 31,7…40,6 |
| Молярная теплоемкость C p жидкого хлора (при -101…-34°С), Дж/(моль·К) | 67,1…65,7 |
| Коэффициент теплопроводности газа при 0°С, Вт/(м·К) | 0,008 |
| Коэффициент теплопроводности жидкого хлора при 30°С, Вт/(м·К) | 0,62 |
| Энтальпия газа, кДж/кг | 1,377 |
| Энтальпия насыщенного пара, кДж/кг | 1,306 |
| Энтальпия жидкого хлора, кДж/кг | 0,879 |
| Показатель преломления при 14°С | 1,367 |
| Удельная электропроводность при -70°С, См/м | 10 -18 |
| Сродство к электрону, кДж/моль | 357 |
| Энергия ионизации, кДж/моль | 1260 |
Плотность хлора
При нормальных условиях хлор представляет собой тяжелый газ, плотность которого приблизительно в 2,5 раза выше . Плотность газообразного и жидкого хлора при нормальных условиях (при 0°С) равна, соответственно 3,214 и 1468 кг/м 3 . При нагревании жидкого или газообразного хлора его плотность снижается из-за увеличения объема вследствие теплового расширения.
Плотность газообразного хлора
В таблице представлены значения плотности хлора в газообразном состоянии при различных температурах (в интервале от -30 до 140°С) и нормальном атмосферном давлении (1,013·10 5 Па). Плотность хлора меняется с изменением температуры — при нагревании она уменьшается. Например, при 20°С плотность хлора равна 2,985 кг/м 3 , а при повышении температуры этого газа до 100°С, величина плотности снижается до значения 2,328 кг/м 3 .
| t, °С | ρ, кг/м 3 | t, °С | ρ, кг/м 3 |
|---|---|---|---|
| -30 | 3,722 | 60 | 2,616 |
| -20 | 3,502 | 70 | 2,538 |
| -10 | 3,347 | 80 | 2,464 |
| 0 | 3,214 | 90 | 2,394 |
| 10 | 3,095 | 100 | 2,328 |
| 20 | 2,985 | 110 | 2,266 |
| 30 | 2,884 | 120 | 2,207 |
| 40 | 2,789 | 130 | 2,15 |
| 50 | 2,7 | 140 | 2,097 |
При росте давления плотность хлора увеличивается . Ниже в таблицах приведена плотность газообразного хлора в интервале температуры от -40 до 140°С и давлении от 26,6·10 5 до 213·10 5 Па. С повышением давления плотность хлора в газообразном состоянии увеличивается пропорционально. Например, увеличение давления хлора с 53,2·10 5 до 106,4·10 5 Па при температуре 10°С приводит к двукратному увеличению плотности этого газа.
| ↓ t, °С | P, кПа → | 26,6 | 53,2 | 79,8 | 101,3 |
|---|---|---|---|---|
| -40 | 0,9819 | 1,996 | — | — |
| -30 | 0,9402 | 1,896 | 2,885 | 3,722 |
| -20 | 0,9024 | 1,815 | 2,743 | 3,502 |
| -10 | 0,8678 | 1,743 | 2,629 | 3,347 |
| 0 | 0,8358 | 1,678 | 2,528 | 3,214 |
| 10 | 0,8061 | 1,618 | 2,435 | 3,095 |
| 20 | 0,7783 | 1,563 | 2,35 | 2,985 |
| 30 | 0,7524 | 1,509 | 2,271 | 2,884 |
| 40 | 0,7282 | 1,46 | 2,197 | 2,789 |
| 50 | 0,7055 | 1,415 | 2,127 | 2,7 |
| 60 | 0,6842 | 1,371 | 2,062 | 2,616 |
| 70 | 0,6641 | 1,331 | 2 | 2,538 |
| 80 | 0,6451 | 1,292 | 1,942 | 2,464 |
| 90 | 0,6272 | 1,256 | 1,888 | 2,394 |
| 100 | 0,6103 | 1,222 | 1,836 | 2,328 |
| 110 | 0,5943 | 1,19 | 1,787 | 2,266 |
| 120 | 0,579 | 1,159 | 1,741 | 2,207 |
| 130 | 0,5646 | 1,13 | 1,697 | 2,15 |
| 140 | 0,5508 | 1,102 | 1,655 | 2,097 |
| ↓ t, °С | P, кПа → | 133 | 160 | 186 | 213 |
|---|---|---|---|---|
| -20 | 4,695 | 5,768 | — | — |
| -10 | 4,446 | 5,389 | 6,366 | 7,389 |
| 0 | 4,255 | 5,138 | 6,036 | 6,954 |
| 10 | 4,092 | 4,933 | 5,783 | 6,645 |
| 20 | 3,945 | 4,751 | 5,565 | 6,385 |
| 30 | 3,809 | 4,585 | 5,367 | 6,154 |
| 40 | 3,682 | 4,431 | 5,184 | 5,942 |
| 50 | 3,563 | 4,287 | 5,014 | 5,745 |
| 60 | 3,452 | 4,151 | 4,855 | 5,561 |
| 70 | 3,347 | 4,025 | 4,705 | 5,388 |
| 80 | 3,248 | 3,905 | 4,564 | 5,225 |
| 90 | 3,156 | 3,793 | 4,432 | 5,073 |
| 100 | 3,068 | 3,687 | 4,307 | 4,929 |
| 110 | 2,985 | 3,587 | 4,189 | 4,793 |
| 120 | 2,907 | 3,492 | 4,078 | 4,665 |
| 130 | 2,832 | 3,397 | 3,972 | 4,543 |
| 140 | 2,761 | 3,319 | 3,87 | 4,426 |
Плотность жидкого хлора
Жидкий хлор может существовать в относительно узком температурном диапазоне, границы которого лежат от минус 100,5 до плюс 144°С (то есть от температуры плавления до критической температуры). Выше температуры 144°С хлор не перейдет в жидкое состояние ни при каком давлении. Плотность жидкого хлора в этом температурном интервале изменяется от 1717 до 573 кг/м 3 .
| t, °С | ρ, кг/м 3 | t, °С | ρ, кг/м 3 |
|---|---|---|---|
| -100 | 1717 | 30 | 1377 |
| -90 | 1694 | 40 | 1344 |
| -80 | 1673 | 50 | 1310 |
| -70 | 1646 | 60 | 1275 |
| -60 | 1622 | 70 | 1240 |
| -50 | 1598 | 80 | 1199 |
| -40 | 1574 | 90 | 1156 |
| -30 | 1550 | 100 | 1109 |
| -20 | 1524 | 110 | 1059 |
| -10 | 1496 | 120 | 998 |
| 0 | 1468 | 130 | 920 |
| 10 | 1438 | 140 | 750 |
| 20 | 1408 | 144 | 573 |
Удельная теплоемкость хлора
Удельная теплоемкость газообразного хлора C p в размерности кДж/(кг·К) в интервале температуры от 0 до 1200°С и нормальном атмосферном давлении может быть рассчитана по формуле:
где T — абсолютная температура хлора в градусах Кельвина.
Следует отметить, что при нормальных условиях удельная теплоемкость хлора имеет значение 471 Дж/(кг·К) и при нагревании увеличивается. Рост теплоемкости при температурах выше 500°С становится незначительным, и при высоких температурах удельная теплоемкость хлора практически не изменяется.
В таблице приведены результаты расчета удельной теплоемкости хлора по указанной выше формуле (погрешность расчета составляет около 1%).
| t, °С | C p , Дж/(кг·К) | t, °С | C p , Дж/(кг·К) |
|---|---|---|---|
| 0 | 471 | 250 | 506 |
| 10 | 474 | 300 | 508 |
| 20 | 477 | 350 | 510 |
| 30 | 480 | 400 | 511 |
| 40 | 482 | 450 | 512 |
| 50 | 485 | 500 | 513 |
| 60 | 487 | 550 | 514 |
| 70 | 488 | 600 | 514 |
| 80 | 490 | 650 | 515 |
| 90 | 492 | 700 | 515 |
| 100 | 493 | 750 | 515 |
| 110 | 494 | 800 | 516 |
| 120 | 496 | 850 | 516 |
| 130 | 497 | 900 | 516 |
| 140 | 498 | 950 | 516 |
| 150 | 499 | 1000 | 517 |
| 200 | 503 | 1100 | 517 |
При температуре близкой к абсолютному нулю хлор находится в твердом состоянии и имеет низкую величину удельной теплоемкости (19 Дж/(кг·К)). По мере увеличения температуры твердого Cl 2 его теплоемкость растет и достигает при минус 143°С величины 720 Дж/(кг·К).
Жидкий хлор имеет удельную теплоемкость 918…949 Дж/(кг·К) в интервале от 0 до -90 градусов Цельсия. По данным таблицы видно, что удельная теплоемкость жидкого хлора выше чем газообразного и при увеличении температуры снижается.
Теплопроводность хлора
В таблице представлены значения коэффициентов теплопроводности газообразного хлора при нормальном атмосферном давлении в интервале температуры от -70 до 400°С.
Коэффициент теплопроводности хлора при нормальных условиях составляет 0,0079 Вт/(м·град), что в 3 раза меньше чем у при тех же температуре и давлении. Нагревание хлора приводит к повышению его теплопроводности. Так, при температуре 100°С, значение этого физического свойства хлора увеличивается до 0,0114 Вт/(м·град).
| t, °С | λ, Вт/(м·град) | t, °С | λ, Вт/(м·град) |
|---|---|---|---|
| -70 | 0,0054 | 50 | 0,0096 |
| -60 | 0,0058 | 60 | 0,01 |
| -50 | 0,0062 | 70 | 0,0104 |
| -40 | 0,0065 | 80 | 0,0107 |
| -30 | 0,0068 | 90 | 0,0111 |
| -20 | 0,0072 | 100 | 0,0114 |
| -10 | 0,0076 | 150 | 0,0133 |
| 0 | 0,0079 | 200 | 0,0149 |
| 10 | 0,0082 | 250 | 0,0165 |
| 20 | 0,0086 | 300 | 0,018 |
| 30 | 0,009 | 350 | 0,0195 |
| 40 | 0,0093 | 400 | 0,0207 |
Вязкость хлора
Коэффициент динамической вязкости газообразного хлора в интервале температуры 20…500°С можно приближенно вычислить по формуле:
где η T — коэффициент динамической вязкости хлора при заданной температуре T, К;
η T 0 — коэффициент динамической вязкости хлора при температуре T 0 =273 К (при н. у.);
С — константа Сюзерленда (для хлора С=351).
При нормальных условиях динамическая вязкость хлора равна 0,0123·10 -3 Па·с. При нагревании такое физическое свойство хлора, как вязкость, принимает более высокие значения.
Жидкий хлор имеет вязкость на порядок выше, чем газообразный. Например, при температуре 20°С динамическая вязкость жидкого хлора имеет величину 0,345·10 -3 Па·с и при росте температуры снижается.
Источники:
- Барков С. А. Галогены и подгруппа марганца. Элементы VII группы периодической системы Д. И. Менделеева. Пособие для учащихся. М.: Просвещение, 1976 — 112 с.
- Таблицы физических величин. Справочник. Под ред. акад. И. К. Кикоина. М.: Атомиздат, 1976 - 1008 с.
- Якименко Л. М., Пасманик М. И. Справочник по производству хлора, каустической соды и основных хлорпродуктов. Изд. 2-е, пер. и др. М.: Химия, 1976 — 440 с.
Элемент VII подгруппы Периодической таблицы Д.И.Менделеева. На внешнем уровне - 7 электронов, поэтому при взаимодействии с восстановителями, хлор показывает свои окислительные свойства, притягивая к себе электрон металла.
Физические свойства хлора.
Хлор представляет собой желтый газ. Имеет резкий запах.
Химические свойства хлора.
Свободный хлор очень активен. Он реагирует со всеми простыми веществами, кроме кислорода, азота и благородных газов:
Si + 2 Cl 2 = SiCl 4 + Q .
При взаимодействии с водородом при комнатной температуре реакции практически нет, но как только освещение выступает в качестве внешнего воздействия, возникает цепная реакция, которая нашла свое применение в органической химии.
При нагреве хлор способен вытеснить йод или бром из их кислот:
Cl 2 + 2 HBr = 2 HCl + Br 2 .
С водой хлор реагирует, частично растворяясь в ней. Эту смесь называют хлорной водой.
Реагирует с щелочами:
Cl 2 + 2NaOH = NaCl + NaClO + H 2 O (холод ),
Cl 2 + 6KOH = 5KCl + KClO 3 + 3 H 2 O (нагрев ).
Получение хлора.
1. Электролиз расплава хлорида натрия, который протекает по следующей схеме:
2. Лабораторный способ получения хлора:
MnO 2 + 4HCl = MnCl 2 + Cl 2 + 2H 2 O.